L’annexe 11 et les systèmes informatisés
Il y a quelques temps je te parlais dans un article, de l’Annexe 1.
Un autre document excessivement important pour toutes activités régies selon les normes BPF est l’Annexe 11. L’Annexe 11 concerne les systèmes informatisés comme les systèmes de monitoring environnemental (AKA EMS).
Trêve de bavardage, je vais laisser la place à Lucas, notre stagiaire, qui va-t’en dire un peu plus sur cette annexe 11 quand il aura terminé son café. Et si tu veux je t’offre un petit aperçu en image juste en-dessous.
L’annexe 11 c’est quoi ?
L’Annexe 11 est un document, qui comme l’Annexe 1, fait partie des directives des bonnes pratiques de fabrication, directives qui sont éditées et publiées par la Commission Européenne.
En bref, lorsqu’un système informatisé remplace une opération manuelle, il ne doit pas en résulter une baisse de la qualité de ton produit, de la maitrise de tes processus ou de l’assurance qualité.
L’annexe 11 côté US, ça donne quoi ?
On compare souvent l’Annexe 11 à la partie 11 du 21 CFR de la FDA, mais attention, l’annexe 11 a une portée beaucoup plus large que la partie 11 américaine.
L’annexe 11 concerne plus que des enregistrements électroniques, elle prend en compte tout le cycle de vie du système informatisé. Elle met l’accent sur l’évaluation des risques en tant qu’outil pour garantir la sécurité et l’efficacité des produits.
L’Annexe 11 – Quels sont les objectifs ?
Tu te doutes donc qu’à partir du moment où un système informatique (notre logiciel Mirrhia, par exemple) remplace des activités manuelles, ce système en question ne peut en aucun cas engendrer une perte de la qualité ni causer de risque. Si tu as déjà entendu parler d’intégrité des données… Et bien on nage en plein dedans.
Elle permet de définir les critères selon lesquels les enregistrements électroniques et les signatures électroniques peuvent être considérés comme équivalent aux documents papiers.
L’annexe 11 et la signature électronique
Concrètement, la signature électronique permet d’identifier de manière certaine l’auteur d’un document électronique, de garantir l’intégrité du contenu du document et de s’assurer que l’auteur ne peut pas nier avoir signé le document. Ces garanties sont essentielles pour assurer la sécurité et la qualité des produits pharmaceutiques fabriqués.
Pour être conforme à l’Annexe 11 de l’Union européenne, la signature électronique doit être réalisée à l’aide d’un certificat électronique valide et d’un moyen d’authentification sûr (par exemple, un mot de passe).
Mirrhia Labs et Mirrhia Facility permettent de gérer la signature électronique.Pour certaines tâches/modifications, la signature électronique est demandée.
C’est-à-dire que Mirrhia demande une identification lors de l’exécution de l’action bien que l’utilisateur soit déjà connecté sur le système. Cette signature remplace la signature manuscrite d’une personne et elle permet d’authentifier l’auteur d’un document ou d’une action et de manière précise et d’en garantir la non-répudiation.
La signature électronique présente dans les logiciel Mirrhia Labs et Mirrhia Facility respecte les 5 règles fondamentales pour une signature électronique fiable :
- L’auteur est facilement identifiable
- Le signataire ne peut pas contester l’avoir signé
- Le signataire ne peut pas se faire passer pour une autre personne
- La signature ne peut pas être utilisée sur un autre document
- Une fois signé, le document n’est pas modifiable et il est archivé de manière automatique
L’annexe 11 et les enregistrements électroniques
Les enregistrements électroniques sont des éléments importants dans la mise en place des bonnes pratiques de fabrication (GMP) pour les produits pharmaceutiques. L’Annexe 11 de l’Union européenne énonce les exigences relatives à la gestion des enregistrements électroniques dans le contexte de la fabrication de produits pharmaceutiques.
Le principe d’ALCOA +
Le principe ALOCA+ est là pour garantir la qualité et la fiabilité de ces enregistrements électroniques.
ALCOA, c’est un concept qui est apparu pour la première fois dans une documentation de la FDA. Cet acronyme est sorti tout droit du cerveau de Stan Woollen de la FDA justement et liste des principes concernant la collecte et la gestion des données. En fait, l’ALCOA est né pour répondre à un problème crucial de négligence volontaire ou involontaire ou encore de mauvaises habitudes pouvant causer l’altération des données, voir la perte de celle-ci.
Et ALCOA, ça veut dire quoi ? Alors on dit que la donnée doit être Attribuable à quelqu’un (d’où la signature électronique décrite au point juste au-dessus), Lisible (traçable et permanente), Contemporaine (émise à une heure et date précise), Originale (sans modification ultérieure) et Accurate (Exacte). La notion d’ALCOA+ précise également que la donnée doit être Complète, Concordante, Durable et Disponible sur un serveur sécurisé.
Tu l’auras compris, garantir l’intégrité des données dans le cadre d’activités relatives à la production de médicaments, c’est un enjeu majeur. Suivre les principes ALACO aide les fabricants à respecter les normes en vigueur.
Mirrhia a conçu toutes ses solutions afin qu’elles respectent scrupuleusement les directives de l’annexe 11.En ce qui concerne les enregistrements électroniques, voyons point par point, concrètement, comment Mirrhia applique ces règles.
Attribuable :
Chaque utilisateur qui utilise l’une de nos solutions possède un compte protégé par un mot de passe.Cet utilisateur possède un rôle précis, ce rôle définis quelles actions l’utilisateur peut effectuer sur le système.
L’administrateur peut restreindre ou augmenter le champ d’action possible de chaque utilisateur.Toutes les actions effectuées sur le système sont consignées dans un audit trail.
Dans cet audit, on peut y retrouver les informations suivantes :
- Quelles actions ont été effectuées
- Sur quel facteur
- Par quel utilisateur
- Pour quelle raison l’action a été effectuée
- Quand l’action a été faite (date et heure)
- Valeur avant et après la modification
Vous l’aurez compris, chaque modification survenue peut donc être liée attribué à une personne.
Lisible :
Les données enregistrées et les alarmes sont consultable en temps réel ou ultérieurement.Nos solutions permettent d’extraire une série de rapports et ce dans plusieurs types de format.
Nous donnons la possibilité de générer des rapports sur chaque donnée entrée dans le système ainsi que chaque modification faite sur le système.Mirrhia permet même d’extraire automatiquement l’EBR (Eletronic Batch Record) relatif aux données environnementales pour un lot donné.
Contemporaine :
L’horodatage (le fait qu’un événement soit associé à une date et à une heure) est entièrement intégré dans nos solutions.
Que ça soit dans nos rapports ou dans les audits, chaque événement sera toujours accompagné de la date et de l’heure à laquelle il est survenu.Pour ce faire, chaque donnée et évènement sont automatiquement enregistrés au moment de l’action avec un horodatage précis.
Originale :
Mirrhia certifie que les données enregistrées dans ses solutions sont issues du premier enregistrement.
Conformément à l’annexe 11, toutes les données entrées dans le système ne peuvent en aucun cas être supprimées ou modifiés.
Accurate :
Mirrhia assure formellement que chaque donnée entrée dans le système est conforme à la réalité et traitée correctement.
Conformément à l’annexe 11 et à l’intégrité des données, aucune donnée ne peut être modifié ou supprimée.Afin de garder une mesure totalement exacte, un système d’ajustage suite à une calibration est disponible dans nos solutions Mirrhia Labs et Mirrhia Facility. Cet ajustage ce base sur un certificat établi selon les normes en vigueur.
À qui l’Annexe 11 s’applique-t ’elle ?
L’Annexe 11 s’applique aux entreprises pharmaceutiques et aux fabricants de médicaments qui opèrent dans l’Union Européenne. Elle s’applique également aux entreprises qui importent des médicaments dans l’UE. Les entreprises doivent s’y conformer pour pouvoir commercialiser leurs produits sur le marché européen.
Comprendre comment s’organise l’annexe 11
L’annexe 11 est composée de 3 grandes phases qui se divisent en 17 contrôles distincts, ces trois phases sont :
- La généralité
- La phase Projet
- La phase opérationnelle
Nous allons passer à travers ses trois phases en décrivant les directives qui les composent.
La phase de généralité
Les trois premiers contrôles forment la partie « général », c’est-à-dire qu’ils sont considérés comme un prélude pour guider la conformité à l’annexe 11.
Les trois directives en question :
La gestion des risques :
- La gestion des risques doit être appliquée tout au long du cycle de vie du système informatisé. Elle prend en compte, la sécurité des patients, l’intégrité des données, et la qualité des produits.
- La coopération étroite ente tout le personnel concerné : Tout le personnel doit avoir la qualification appropriée, leurs niveaux d’accès et leurs responsabilités doivent être clairement définies.
La phase projet
Après la phase de généralité vient la phase projet, appelée également phase de « validation ». Dans l’annexe 11, la validation est considérée comme une activité qui se fait en continu.
C’est-à-dire qu’elle se déroule tout au long du cycle de vie d’un système, de la mise en œuvre au retrait, y compris le contrôle des modifications au fur et à mesure que des mises à jour sont apportées au système.L’annexe 11 prévoit que le fabricant doit être capable de justifier leurs standards, leurs protocoles, leurs critères d’acceptation, leurs procédures et leurs enregistrements, sur la base de leur évaluation du risque.
La phase opérationnelle
Après avoir posé les bases de la mise en conformité des systèmes informatisés avec validation, l’annexe 11 passe à la phase opérationnelle (ou d’exploitation) qui est détaillée par 13 contrôles.
Les deux premiers contrôles se concentrent sur les données entrant dans le système :
- Contrôles intégrés : Lorsque des données sont échangées avec d’autres systèmes, des contrôles intégrés sont nécessaires pour garantir l’exactitude des données et un transfert sécurisé
- Une vérification de précision : Lorsque des données sont introduites manuellement, il est nécessaire de prévoir un contrôle supplémentaire pour vérifier l’exactitude de celles-ci.Ce contrôle supplémentaire peut être faire fait par un deuxième opérateur ou par des moyens électroniques validés.
L’annexe 11 et l’intégrité des données
C’est un des points les plus sensibles de l’annexe 11, la fameuse intégrité des données ou data integrity que tu entendras souvent même dans la langue de Molière.
Trois contrôles se concentrent sur l’accès aux données et sur les protections qui garantissent l’intégrité des données.
- Le stockage des données : Il est nécessaire que celui soit protégé contre les dommages, tout en restant accessible, lisible et exacte tout au long de la période de conservation.Il est préconisé d’effectuer des sauvegardes régulières des données pertinentes, l’intégrité et l’exactitude des données sauvegardées doivent être vérifiées pendant la phase de validation.
- Sorties imprimées : il doit pouvoir être possible d’obtenir des copies imprimées claires des données stockées électroniquement.Pour les données nécessaires à la libération des lots, il doit être possible de générer des impressions indiquant si l’une ou plusieurs d’entre elles ont été modifiées depuis leur saisie initiale.
- Traçabilité des modifications : Sur base d’une analyse de risques, toute modification intervenue sur les données/systèmes doit pouvoir être documentée. L’audit trail doit être disponible, convertible dans un format compréhensible et revu à fréquence régulière.
L’annexe 11 et la sécurité du système
La sécurité du système est également un point central abordé dans l’annexe 11. En bref, des moyens physiques et/ou logiques doivent être mis en place afin de restreindre l’accès des systèmes informatisés au seul personnel autorisé.
Différentes méthodes adéquates peuvent être mises en place telle l’utilisation de clés, de badges, de codes personnels associés à des mots de passe, de la biométrie etc…En bref, l’étendue des contrôles de sécurité dépend de la criticité du système informatisé.La modification, l’annulation et la création des autorisations d’accès doivent être enregistrées.
L’annexe 11 et le contrôle de gestion de qualité
Dans cette partie, se retrouvent les contrôles qui garantissent qu’un système dispose d’un support connu pour un fonctionnement continu dans un état validé et contrôlé.
- Maitrise des changements et de la configuration : toute modification d’un système informatisé, y compris relative à sa configuration, ne peut être réalisée que de façon maitrisée et conformément à une procédure définie.
- Evaluation périodique : Les systèmes informatisés doivent périodiquement faire l’objet d’une évaluation afin de s’assurer qu’ils restent dans un état validé et conforme au BPF. L’annexe 11 prévoit que ces évaluations doivent inclure la gamme en cours de fonctionnalités, les enregistrements des déviations, les incidents, les problèmes historiques des mises à jour et les rapportes de performance, de fiabilité, de sécurité et de validation.
- Gestion des incidents : tous les incidents, pas seulement ceux liés aux défaillances du système et aux erreurs de données, doivent pouvoir être rapporté et évalué.L’origine d’un incident critique doit pouvoir être identifié afin de pouvoir constituer la base d’actions correctives et préventives.
- La continuité opérationnelle : Des dispositions doivent être prises afin d’assurer le bon fonctionnement des procédés critiques même lors de panne.Ces arrangements alternatifs doivent être correctement documentés et testés.
Un consensus international en approche
Donc on a parlé ci-dessus de l’annexe 11 et du 21 CFR part 11.
Sache que les autorités japonaises ont également publié un guide (Guideline on Management of Computerized Systems for Marketing Authorization). La chine en a fait de même avec une version assez proche de notre version européenne (China FDA GMP Annex – Computerised systems).
Il faut quand même signaler qu’une volonté d’harmoniser tout ça est bien présente.
Parlons quelques instants du PIC/S (Pharmaceutical Inspection Co-operation Scheme) qui est une organisation internationale regroupant des autorités réglementaires pharmaceutiques du monde entier pour harmoniser les normes d’inspection et de réglementation dans l’industrie pharmaceutique. Les membres de PIC/S coopèrent pour établir des normes élevées de qualité, de sécurité et d’efficacité des médicaments, ainsi que pour promouvoir l’application cohérente de ces normes parmi les autorités réglementaires. Les activités de PIC/S comprennent l’élaboration de normes, la formation des inspecteurs, l’échange d’informations et la coopération technique entre les membres.
Citons également le GAMP 5 (Good Automated Manufacturing Practice) qui est un ensemble de lignes directrices internationales (non réglementaire) pour la validation des systèmes informatisés utilisés dans l’industrie pharmaceutique et des sciences de la vie. Il fournit un cadre pour l’assurance de la qualité et la gestion des risques associés aux systèmes automatisés utilisés dans la fabrication de produits pharmaceutiques. Le document GAMP 5 est publié par l’International Society for Pharmaceutical Engineering (ISPE) et intègre toutes les exigences du PIC/S.
Si tu veux en savoir plus sur la nouvelle version de l’Annexe 1 qui est sortie au mois d’aout 2022. N’hésite pas à lire notre article Annexe 1 – Nouvelle version. Et puis si tu es curieux, je t’invite également à lire l’Annexe 1 pour les nuls, si tu veux avoir un premier aperçu de ce qu’est ce document et du pourquoi il existe.
Envie de discuter avec notre team Mirrhia ?
Donc si tu veux papoter avec nous de nos solutions Mirrhia, tu peux nous contacter et nous serons ravis de discuter de tes projets.
La minute de Marie
Découvre la minute de Marie » sur l’EMS dans le Pharma?

Automatisation avancée en salle blanche
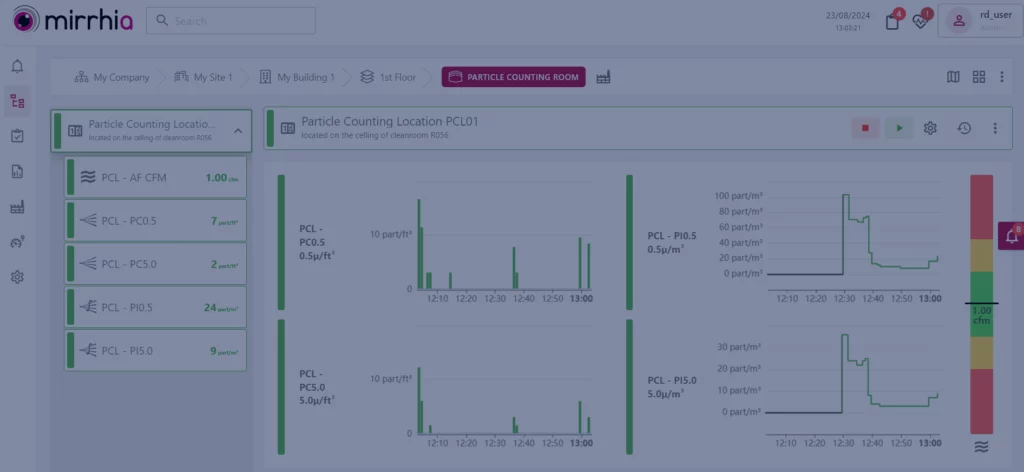
Mirrhia 2.5 est là !

Omega, le partenaire italien de Mirrhia, mis à l’honneur dans Genova Impresa

Arrivée d’Etienne Van den Bogaert en tant que Managing Director
Mirrhia 2.4 arrive

L’intégrité des données dans l’industrie pharmaceutique

Laborama 2024

Monitoring de température et d’humidité en laboratoire
